Cell:脂肪酸通过影响阴道菌群改善女性生殖健康
时间 : 2024-08-25
论文《Vaginal Lactobacillus fatty acid response mechanisms reveal a metabolite-targeted strategy for bacterial vaginosis treatment》发表于《Cell》,作者为 Meilin Zhu 等人。该研究揭示了阴道乳酸杆菌对脂肪酸的反应机制,并提出了一种基于代谢物的细菌性阴道病(BV)治疗策略。
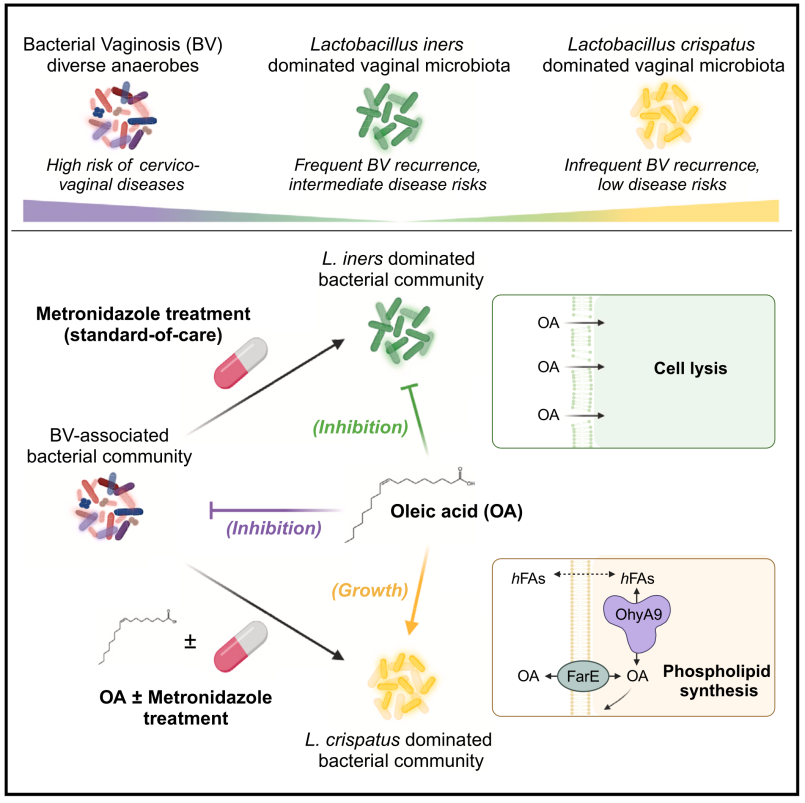
BV 是一种常见的阴道综合征,与不良健康后果相关,其特征是乳酸杆菌缺乏的阴道微生物群和多种厌氧菌的优势。目前的抗生素治疗 BV 效果不佳,易复发,且可能导致阴道微生物群组成向不利于健康的方向转变。
哺乳动物黏膜表面富含长链脂肪酸(LCFAs),其对女性生殖道乳酸杆菌的影响尚未被系统评估。
研究内容和结果:
cis - 9 - uLCFAs 对阴道乳酸杆菌的影响:
顺式 - 9 - 不饱和长链脂肪酸(cis - 9 - uLCFAs),如油酸(OA)、亚油酸(LOA)和棕榈油酸(POA),能抑制乳酸杆菌(L. iners)的生长,而对其他健康相关的乳酸杆菌,如脆乳杆菌(L. crispatus)、加氏乳杆菌(L. gasseri)、詹氏乳杆菌(L. jensenii)和穆氏乳杆菌(L. mulieris)几乎没有抑制作用,甚至能促进它们的生长。
通过转录组和基因组分析,发现非 L. iners 的乳酸杆菌物种具有一组保守的 OA 诱导基因,包括油酸水合酶(ohyA)和一种假定的脂肪酸外排泵(farE),而 L. iners 缺乏这些基因。
对乳酸杆菌 OhyA 酶的功能表征显示,它在体内具有活性,且非 L. iners 的乳酸杆菌能够利用 OhyA 将 OA 转化为 10 - 羟基硬脂酸(10 - HSA),并将其用于磷脂合成,从而在竞争中获得优势。
FGT 乳酸杆菌的脂肪酸代谢:
FGT 乳酸杆菌基因组预测显示,它们缺乏完整的脂肪酸合成 II(FASII)途径,是脂肪酸营养缺陷型,需要外源 LCFAs 如 OA 来构建细胞膜。
非 L. iners 的乳酸杆菌能够利用 OhyA 将 10 - HSA 转化为 OA,从而实现对 OA 的生化营养隔离,这为它们在竞争中提供了优势。
OA 对 BV 相关细菌的影响:
OA 能抑制多种与 BV 相关的非乳酸杆菌细菌的生长,包括对甲硝唑(MTZ)耐药的菌株。
在体外 BV 模型实验中,OA 能单独或与 MTZ 联合使用,使 BV 样细菌群落向 L. crispatus 优势的方向转变。
研究结论和意义:
该研究揭示了 FGT 乳酸杆菌物种在脂肪酸代谢方面的重要种间差异,阐明了其背后的机制,并提出了一种基于代谢物的 BV 治疗策略。
通过促进 L. crispatus 的生长、抑制 L. iners 和许多 BV 相关物种的生长,OA 和相关分子有望改善 BV 的治疗。
讨论:
-
对乳酸杆菌代谢的理解:
-
uLCFA 的抗菌特性:研究发现的 uLCFA(如 OA)对 L. iners 的抑制作用,增加了对 uLCFA 抗菌性质的理解,与其他研究中报道的 uLCFA 对革兰氏阳性菌的抗菌作用一致。
-
OhyA 和 FarE 的作用:非 - iners 的 FGT 乳酸杆菌中保守的 cis - 9 - uLCFA 反应机制,涉及 OhyA、FarE 和 TetR,这与其他生物体中脂肪酸外排泵提供 LCFA 抗性的机制相关,表明 OhyA 和 FarE 在乳酸杆菌应对 LCFA 环境中起着重要作用。
-
乳酸杆菌的营养需求:FGT 乳酸杆菌是脂肪酸营养缺陷型,需要从环境、宿主或其他微生物中获取外源 LCFAs,如 OA,这揭示了它们重要的营养需求和代谢生态位特征。
-
-
对细菌性阴道病治疗的启示:
-
OA 的治疗潜力:OA 能抑制关键的 BV 相关细菌,包括 MTZ 耐药菌株,同时能促进 L. crispatus 生长并抑制 L. iners,这表明 OA 及其相关分子在改善 BV 治疗方面具有潜力。
-
联合治疗的可能性:结合局部应用 OA 和 / 或其他 uLCFA 代谢物与 MTZ,或与微生物群移植或含 L. crispatus 的活菌生物治疗剂联合使用,可能提高治疗效果,促进 L. crispatus 生长并抑制其他物种的竞争。
-
-
研究的局限性:
-
细菌遗传操作的限制:仅在 L. gasseri 中进行了细菌遗传操作,关于 farE 和 ohyA9 在 L. crispatus 中的作用是推断得出的,且缺乏在 L. iners 中异源表达 uLCFA 诱导基因的遗传工具。
-
动物模型的缺乏:由于缺乏人类 FGT 乳酸杆菌定植和 BV 的动物模型,该研究使用了体外模型评估 OA 和 10 - HSA 在群落竞争实验中的效果,人体试验将是全面评估 uLCFA 治疗效果的必要手段。
-
uLCFA 浓度的影响因素:该研究揭示了外源 uLCFAs 的治疗潜力,但原生 FGT 中 uLCFAs 的浓度如何影响微生物群组成,以及饮食、阴道卫生产品或其他遗传或环境因素是否会影响 FGT 中 uLCFAs 的浓度,从而影响乳酸杆菌的定植,这些仍有待确定。
-
-
未来的研究方向:
-
进一步研究 OhyA 酶在宿主 - 微生物和微生物 - 微生物相互作用中的作用,以及它对耐受宿主信号的影响。
-
开展人体试验,全面评估 uLCFA 治疗对 FGT 微生物群的影响。
-
探究影响 FGT 中 uLCFAs 浓度的因素,以及这些因素如何通过改变乳酸杆菌的定植来影响生殖健康。
-



