Cell|癌症中的细胞衰老:标志、悖论与治疗前景
时间 : 2026-04-17
-
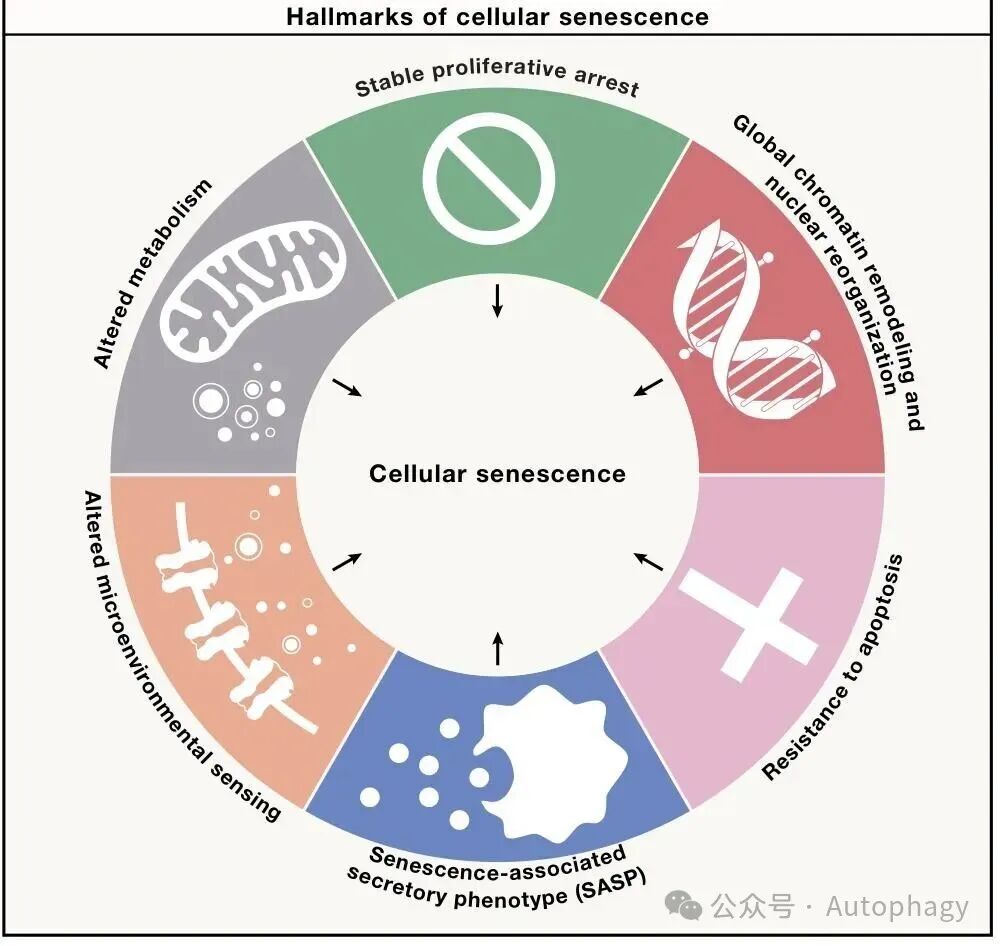
稳定增殖停滞:由 p53/p21、p16INK4a/RB 通路介导,不可逆锁死细胞分裂,区别于可逆的静息状态 -
染色质与核重塑:形成衰老异染色质灶(SAHF)、核纤层结构改变,重塑转录调控格局 -
抗细胞死亡:上调 BCL-2 等抗凋亡蛋白,抵抗凋亡、铁死亡,实现长期存活 -
衰老相关分泌表型(SASP):分泌细胞因子、生长因子、基质酶,主导胞间通信 -
微环境感知重塑:细胞膜表面受体重排,改变免疫识别与胞外信号响应 -
代谢重编程:线粒体 / 溶酶体功能改变、氧化还原失衡,支撑衰老细胞生存
-
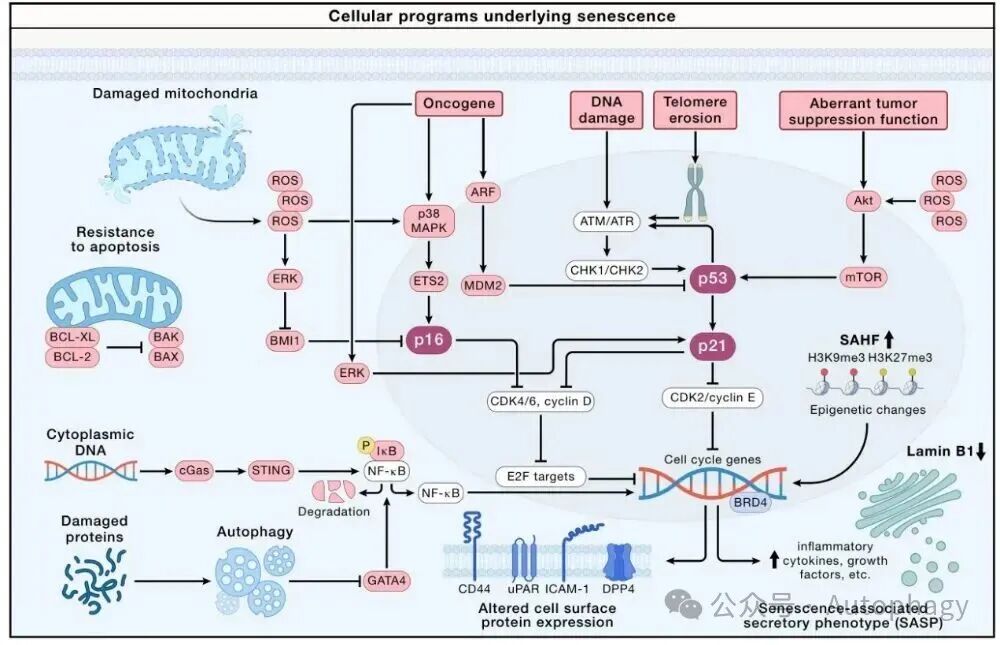
增殖停滞:p53-p21 与 p16-RB 通路双轴驱动,抑制 E2F 转录,关闭细胞周期基因 -
SASP 激活:NF-κB、BRD4、mTOR 等通路主导,独立于周期调控,实现炎症与基质重塑
-
癌基因诱导衰老(OIS)直接阻断癌前细胞恶性转化 -
激活 p53/p16 通路强制停止异常增殖 -
SASP 招募免疫细胞,清除癌前病变细胞
-
衰老细胞长期堆积,SASP 从 “卫士” 变 “恶棍” -
促血管生成、基质降解,助力肿瘤侵袭转移 -
制造免疫抑制微环境,导致治疗耐药与复发
-
胚胎发育:参与肢体、内耳等组织塑形,完成后被巨噬细胞清除 -
组织修复: transient 衰老促进伤口愈合、肝纤维化消退、血管重塑 -
细胞可塑性调控:限制异常细胞重编程,维持组织稳态
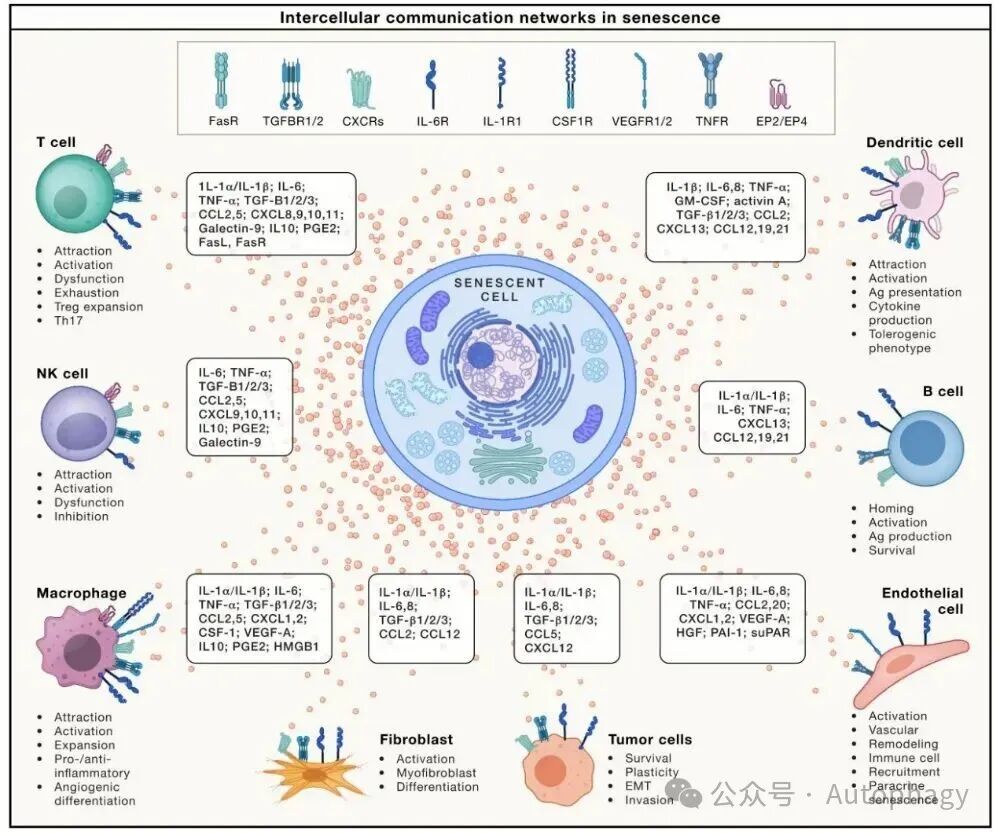
-
加速机体衰老:引发肺纤维化、关节炎、神经退行性病变等老年病 -
放化疗损伤:治疗诱导的正常细胞衰老,导致毒副作用与 “早衰” -
促肿瘤微环境:衰老相关成纤维细胞(CAFs)驱动免疫抑制、肿瘤侵袭



