Cancer Cell:癌症会加速T细胞和组织衰老
时间 : 2025-08-22衰老会大大增加癌症患病风险,并对免疫系统的功能和构成产生深远影响,导致对慢性及急性感染的免疫反应受损,以及易患自身免疫疾病。
那么,癌症本身会加速衰老吗?
2025 年 8 月 21 日,莫菲特癌症中心及研究所的研究人员在 Cancer Cell 上发表了题为:Lymphoma accelerates T cell and tissue aging 的研究论文。
该研究在小鼠和人类中研究发现,淋巴瘤会加速 T 细胞和组织衰老。

衰老导致的免疫系统变化众多,包括炎症细胞因子和趋化因子失衡(炎症衰老)以及分泌表型的变化、造血干细胞向单核细胞群生成的倾斜以及淋巴细胞群的减少、巨噬细胞向促炎极化的转变,以及 NK 细胞和 CD8+ 和 CD4+ T 细胞数量的减少以及成熟度的改变,其中 CD8+ 和 CD4+ T 细胞向功能减弱或免疫抑制性细胞(例如 Treg)转变。
与这些衰老变化相关的是,T 细胞表现出衰老标志物(例如 KLRG1、细胞周期抑制剂 p16INK4a/CDKN2A 以及某些促炎细胞因子)表达增加。最后,衰老的 T 细胞在经历稳态增殖后可能会表现出一些活化标志物 ,但与年轻的活化 T 细胞相比,在生物学和功能上具有独特性。
肿瘤通过施加多种压力以逃避免疫监视。例如,实体瘤的酸性环境会损害 CD8+ T 细胞,却有利于调节性 T 细胞(Treg)的扩增,并促使巨噬细胞向促肿瘤生长的 M2 表型极化。此外,肿瘤微环境中的 T 细胞,尤其是在实体瘤中,会反复受到抗原刺激,从而进入低反应性、功能耗竭的状态。最后,一些肿瘤细胞会抑制 MHC1 的表达以躲避 T 细胞的识别,以及/或者表达 PD-L1 和 CD47 分别来抑制 T 细胞的功能和防止被吞噬。
尽管衰老和癌症对免疫系统有着深远的影响,但它们对免疫细胞命运和功能的共同作用尚不清楚。大多数评估免疫系统影响的研究都集中在癌症治疗上,这些治疗会加速小鼠和人类的衰老,尤其对年轻者影响更大。例如,放射会引发衰老相关 DNA 损伤和甲基化模式,而骨髓移植和化疗会增加血液系统恶性肿瘤患者体内的衰老相关基因 CDKN2A 的表达。此外,儿童、青少年及年轻成年人癌症幸存者已被证实会经历加速衰老,这在很大程度上归因于他们的治疗。但目前尚不清楚癌症本身是否足以加速衰老。
在这项最新研究中,研究团队在年轻小鼠和老年小鼠(均患有 B 细胞淋巴瘤)中探索了衰老和癌症对免疫细胞的综合影响,还在年轻和老年 B 细胞淋巴瘤人类患者中探索了衰老和癌症对 T 细胞的影响。
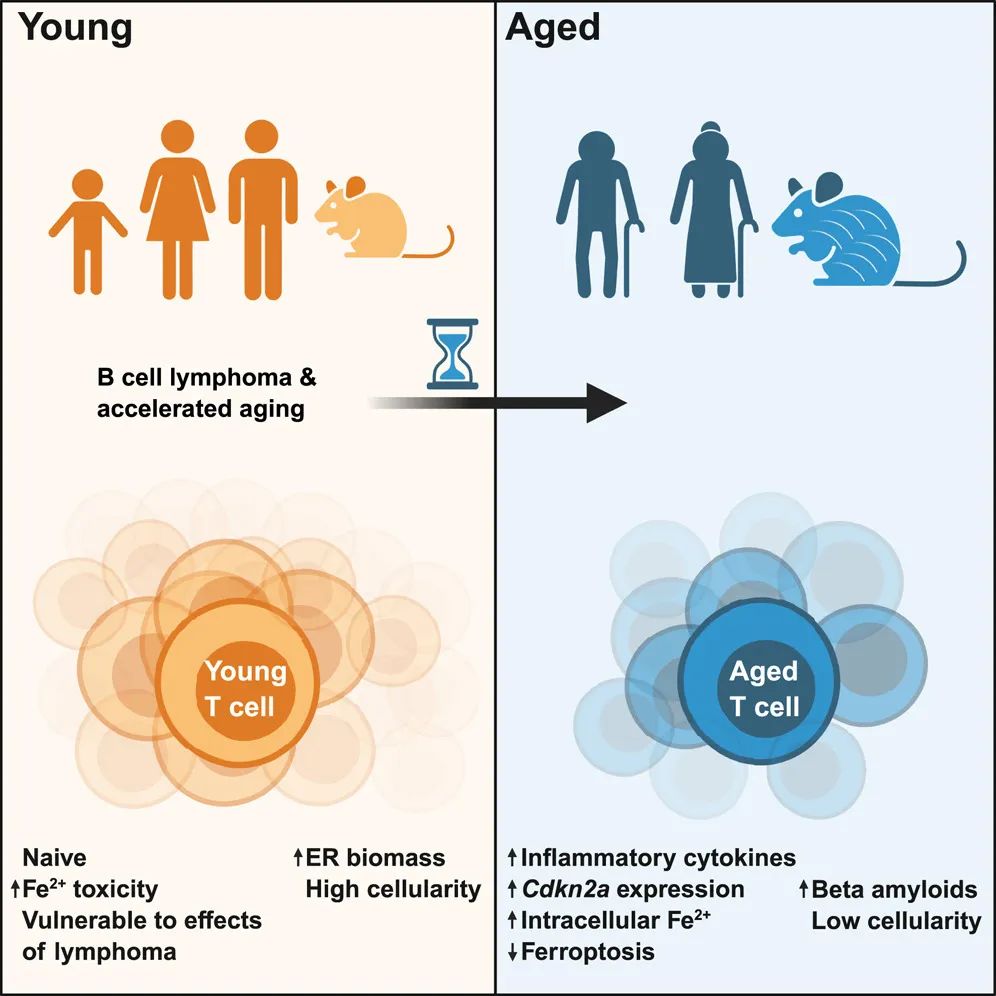
结果表明,淋巴瘤本身足以引发年轻 T 细胞出现转录、表观遗传和表型的改变,这些改变在老年 T 细胞中有所体现。相比之下,衰老的 T 细胞对淋巴瘤诱导的变化具有很强的抵抗力。通路分析显示,开放染色质区域和控制铁稳态的基因均会因淋巴瘤和衰老而被诱导,且经历过淋巴瘤和衰老的 T 细胞铁储备增加,并对铁死亡具有抗性。此外,衰老的 T 细胞和经历过淋巴瘤的 T 细胞在蛋白质稳态方面都存在缺陷。此外,淋巴瘤还会加速其他组织的老化,这从细胞周期蛋白依赖性激酶抑制剂 2a(Cdkn2a)和肿瘤坏死因子α(Tnfa)表达水平的升高可以得到证明。最后,研究团队发现,一些由淋巴瘤引发的衰老表型是可逆的,而另一些则是不可逆的,这表明有机会改善一些与癌症相关的衰老共病。
该研究的核心发现:
-
衰老赋予了对 B 细胞淋巴瘤在年轻 T 细胞中引发的变化的抵抗力;
-
淋巴瘤会加速年轻 T 细胞和组织的衰老;
-
淋巴瘤驱动了衰老 T 细胞中存在的转录和表观遗传特征;
-
淋巴瘤会引发年龄相关炎症,并改变蛋白质和铁稳态。