炎症反应失调是各种炎症性疾病发病机制的主要诱因,例如脓毒症、急性肠道炎症等。最近,发现了一种新型的炎症性程序性细胞死亡,称为细胞焦亡。它是由经典和非经典炎症小体的激活触发的,特别是通过NLRP3炎症小体激活,已成为炎症性疾病的一种有前途的治疗策略。由于GSDMD是一种新发现的炎症小体激活下游的焦亡执行者,因此人们越来越关注将GSDMD作为减轻焦亡疾病的新治疗靶点。
2024年2月7日,四川大学华西医院叶昊宇、杨建洪及吴文爽团队在Science Advances(IF:13.6)发表了题为“NU6300 covalently reacts with cysteine-191 of gasdermin D to block its cleavage and palmitoylation”的文章,该研究通过对化合物库进行了筛选,发现NU6300是细胞焦亡的有效抑制剂。从机制上讲,NU6300共价修饰GSDMD中的C191以阻止其裂解和棕榈酰化,导致随后的GSDMD膜定位障碍。此外,研究证明NU6300给药可改善结肠炎和脓毒症,有望作为炎症性疾病的潜在干预措施。

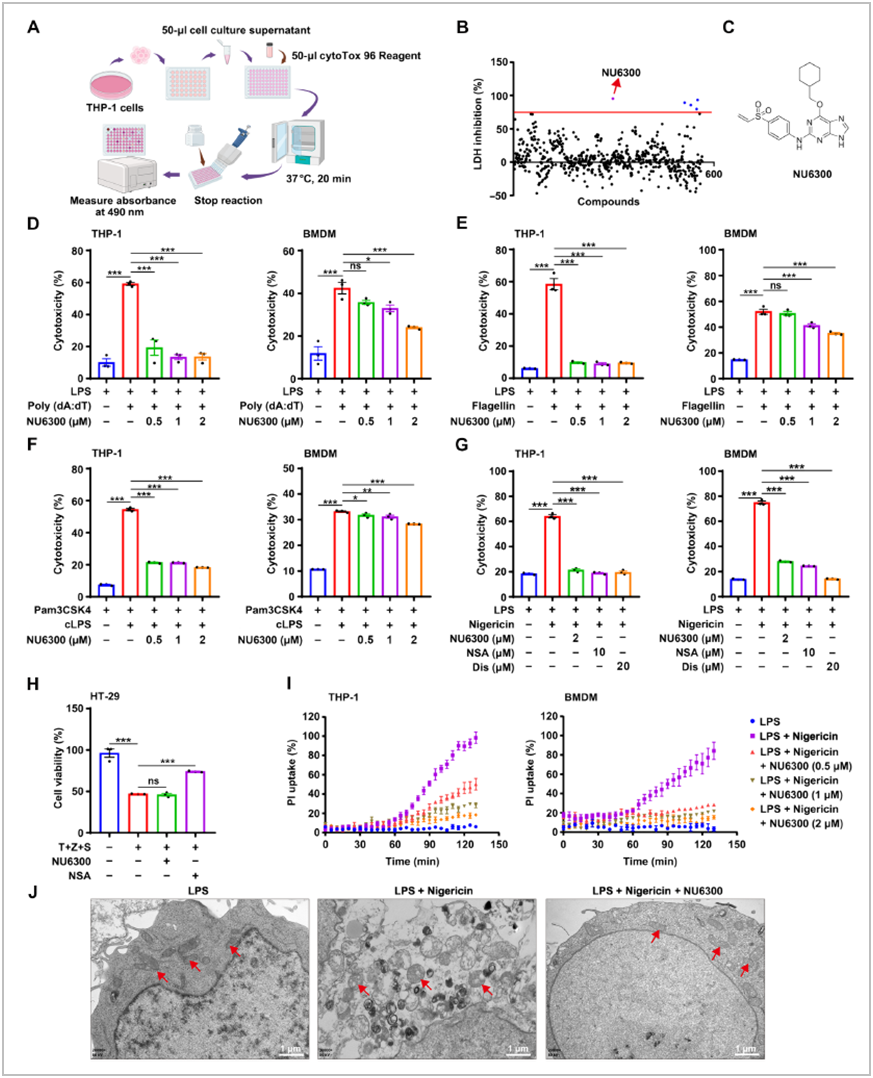
研究利用脂多糖(LPS)+尼日利亚菌素诱导THP-1细胞焦亡进而检测乳酸脱氢酶(LDH)的释放,对包含565种化合物的共价化合物库进行了筛选来确定细胞焦亡的抑制剂。发现NU6300对细胞焦亡表现出剂量依赖性的拯救作用,此外,NU6300阻断了AIM2或 NLRC4炎性体驱动的细胞死亡,除了典型炎症小体之外,NU6300还抑制THP-1细胞和BMDM中非典型炎症小体介导的细胞焦亡。碘化丙啶(PI)摄取测定、活细胞成像、透射电子显微镜分析均显示NU6300减轻了细胞焦亡相关的特征。总的来说,结果表明NU6300可以有效抑制人类和小鼠细胞中典型或非典型炎症小体引发的细胞焦亡(图1)。
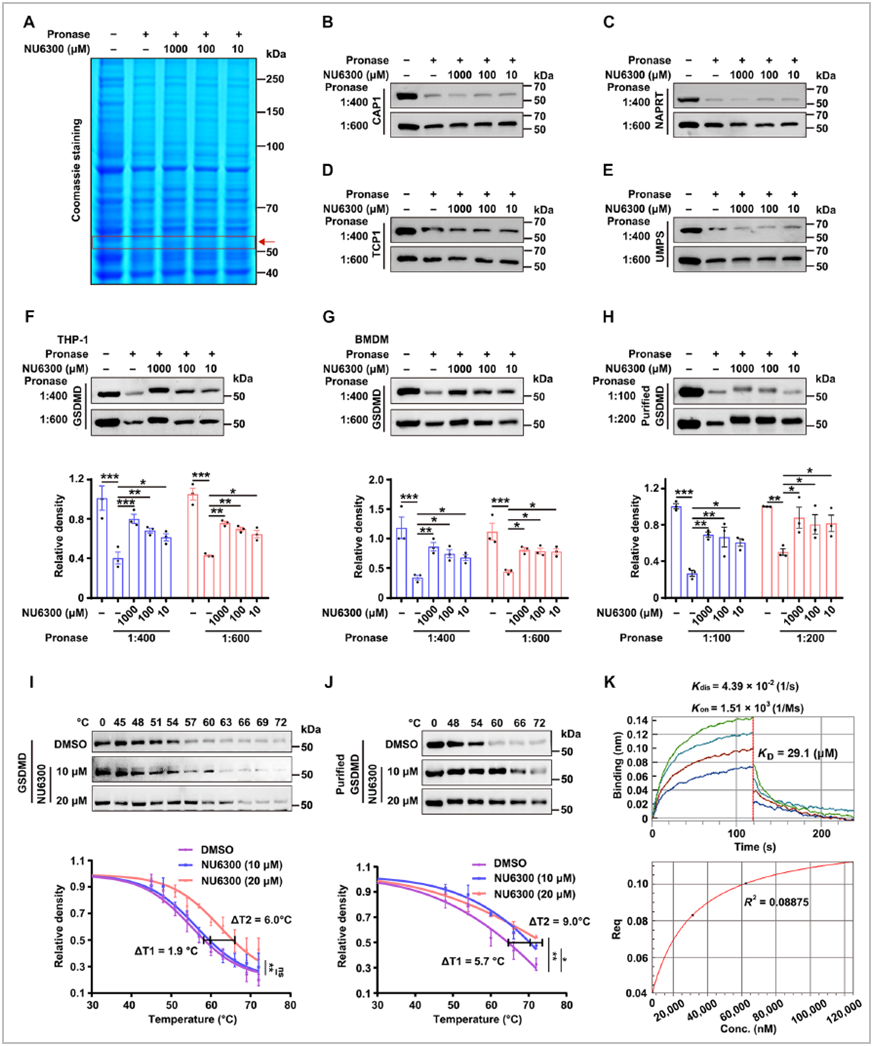
为了研究NU6300在细胞焦亡中的潜在靶点,研究使用THP-1细胞的蛋白裂解物进行了药物亲和力响应靶点稳定性(DARTS)检测,质谱(MS/MS)检测焦亡相关蛋白GSDMD等蛋白为可能的靶蛋白。随后通过对质谱鉴定的首选靶标(CAP1、NAPRT、TCP1、UMPS和GSDMD)进行了免疫印迹,确认NU6300有效保护 GSDMD免遭蛋白酶水解。随后的细胞热位移测定(CETSA)和热位移测定(TSA)、生物层干涉测量(BLI)等结果均证实了GSDMD是NU6300在细胞焦亡中的直接靶标(图2)。
3、NU6300与GSDMD的C191发生共价反应
之前的报道表明,NU6300通过其乙烯基砜部分与CDK2的Lys89发生共价反应。鉴于乙烯基砜是一种亲电子试剂,能够与半胱氨酸或赖氨酸等残基发生共价反应,研究假设NU6300可以与GSDMD发生共价反应。随后研究通过通过将重组人GSDMD蛋白与NU6300一起孵育后质谱鉴定发现NU6300共价修饰在GSDMD的C191上,此外,C56和C268上也检测到修饰。竞争性结合测定证实NU6300靶向结合半胱氨酸。由于这三个半胱氨酸均位于GSDMD的N端(p30),通过在p30片段内的几个保守的人类半胱氨酸(C38、C56、C191 和 C268)中引入半胱氨酸到丙氨酸的突变,p30片段上的C191A突变显著减少了细胞死亡,而C38A、C56A和C268A突变对细胞毒性没有影响。此外,微量热泳(MST)分析进一步表明NU6300与GSDMD C191A没有直接结合。总的来说,C191是共价修饰的重要位点,NU6300与C56和C268的结合是非特异性的,不会影响GSDMD的功能(图3)。
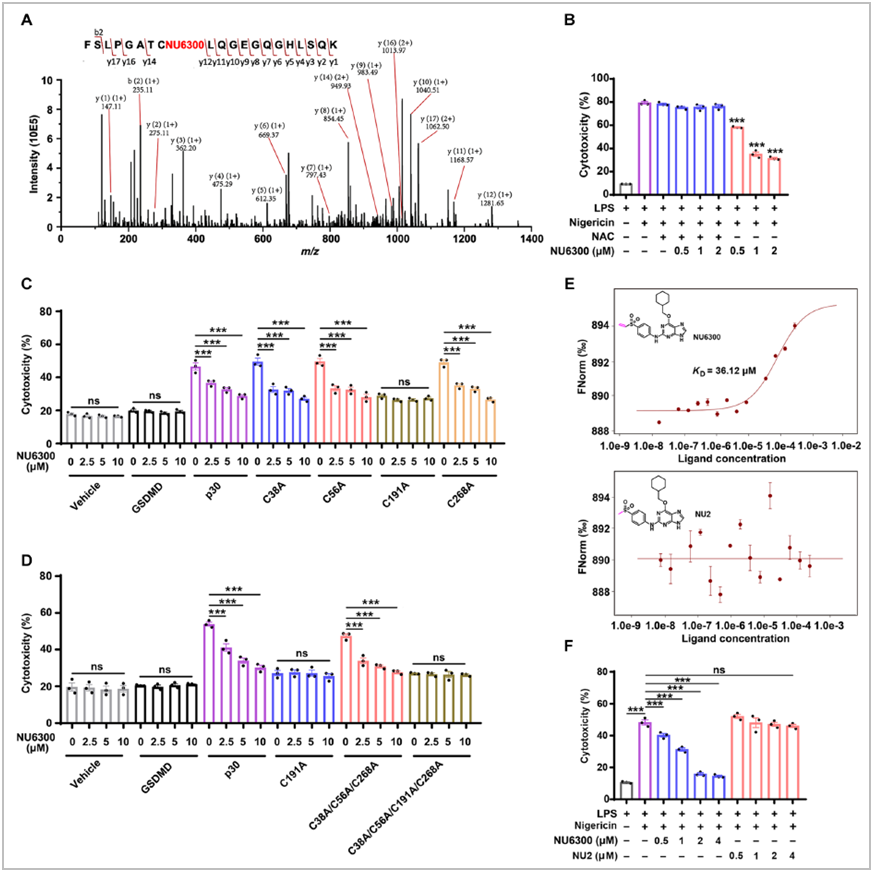
图3 NU6300与GSDMD的C191发生共价反应
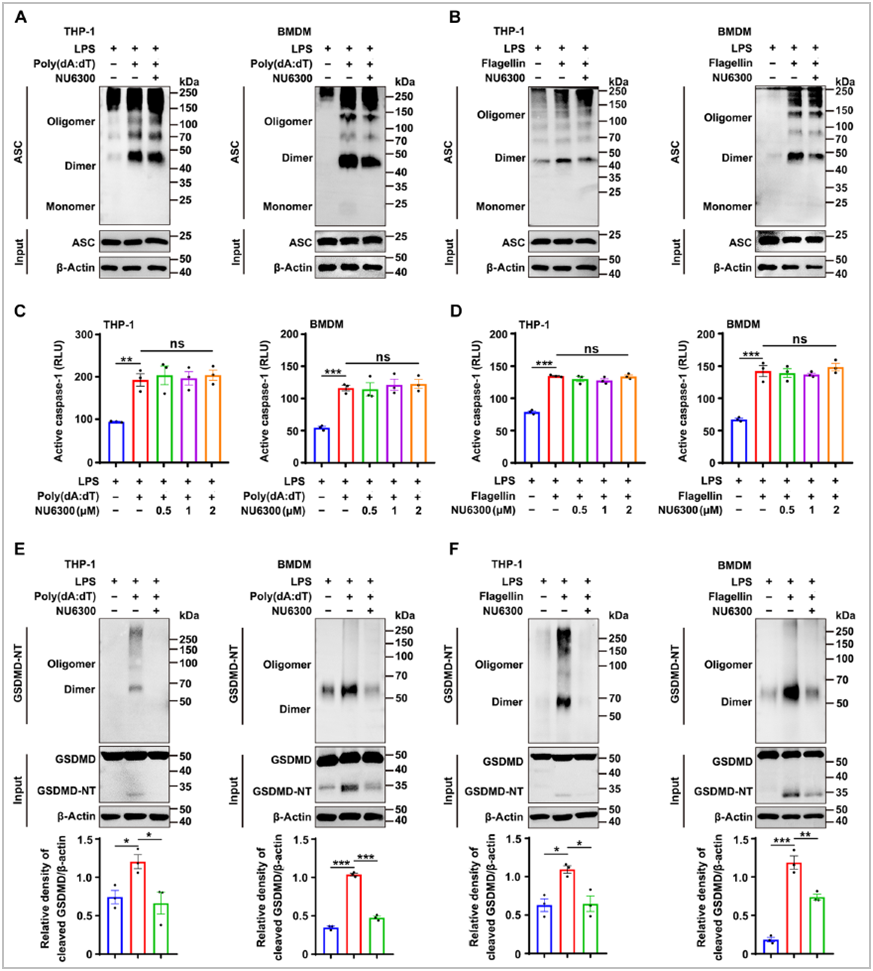
为了确定NU6300对炎性体-GSDMD信号中的GSDMD是否具有选择性,作者研究了NU6300对早期步骤的影响。发现NU6300对AIM2、NLRC4和非经典炎症小体中的ASC寡聚化没有或仅有微弱的抑制作用,并且对AIM2和NLRC4炎症小体中的caspase-1激活没有影响,而NU6300明显阻断了AIM2和NLRC4炎症小体中GSDMD的裂解,证明了NU6300对GSDMD的选择性(图4)。
最近的数据表明,C191的棕榈酰化是GSDMD膜易位和孔形成的必要条件。作者进一步研究了NU6300是否对GSDMD的棕榈酰化起作用。结果发现NU6300显著阻断AIM2和NLRC4炎性体中全长GSDMD的棕榈酰化水平,并且还显著抑制转染GSDMD-N的HEK-293T细胞中GSDMD-N的棕榈酰化水平。进一步研究揭示了NU6300对这两种炎症小体中GSDMD-N易位的抑制作用。总之,NU6300共价修饰GSDMD的C191,阻断其裂解和棕榈酰化,从而抑制 GSDMD-N 膜易位和进一步寡聚化(图5)。
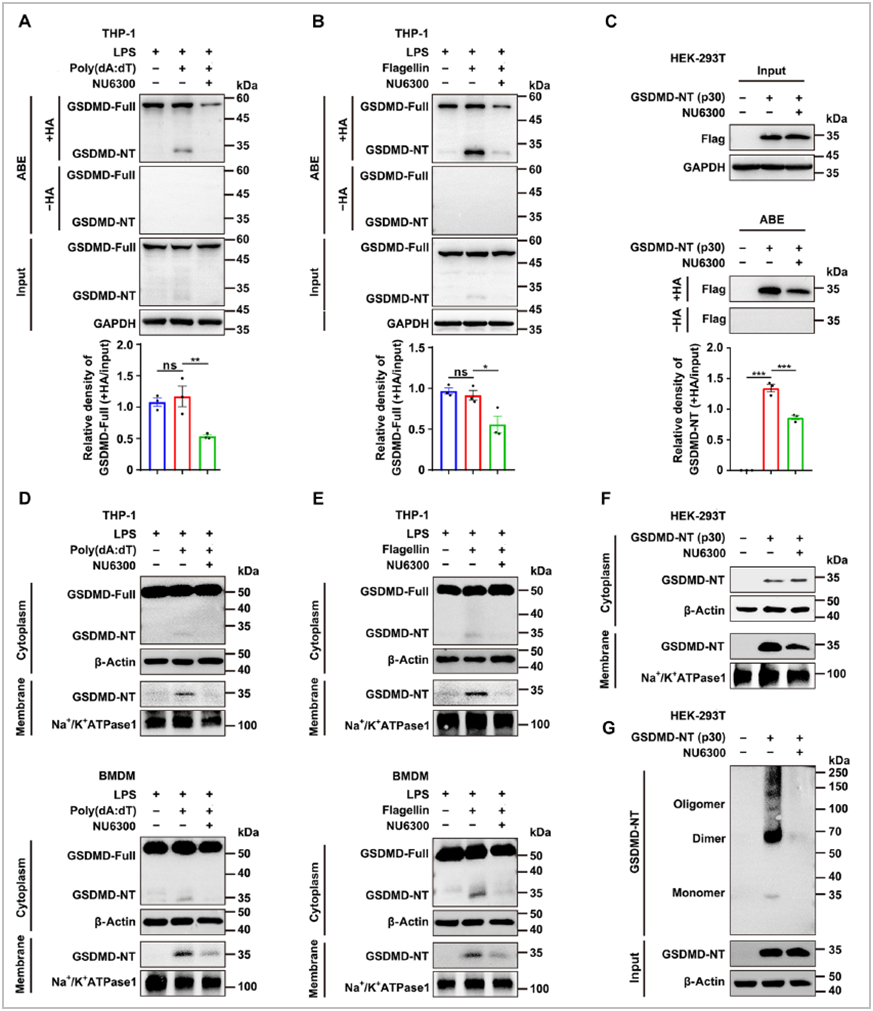
图5 NU6300阻断GSDMD-N的棕榈酰化和膜易位
5、 GSDMD抑制剂对NLRP3炎症小体表现出反馈抑制作用
NU6300对NLRP3炎症小体的早期步骤表现出相当强的抑制作用,对尼日利亚霉素触发的NLRP3炎症小体中的ASC寡聚、caspase-1激活、GSDMD裂解、膜转位以及IL-1β的释放有显著的抑制作用。这些结果促使我们研究NU6300是否也靶向NLRP3或caspase-1。然而DARTS和SPR检测没有观察到NU6300和NLRP3和caspase-1蛋白之间有直接结合。研究进一步发现NU6300 和其他两种已知的GSDMD抑制剂(NSA和Dis)对ASC寡聚化以及 pro-caspase-1、pro-IL-1β和GSDMD的裂解均表现出显著抑制作用。这些结果表明,当抑制GSDMD时,NLRP3炎症小体存在共同的反馈抑制作用,这与之前的研究一致(图6)。
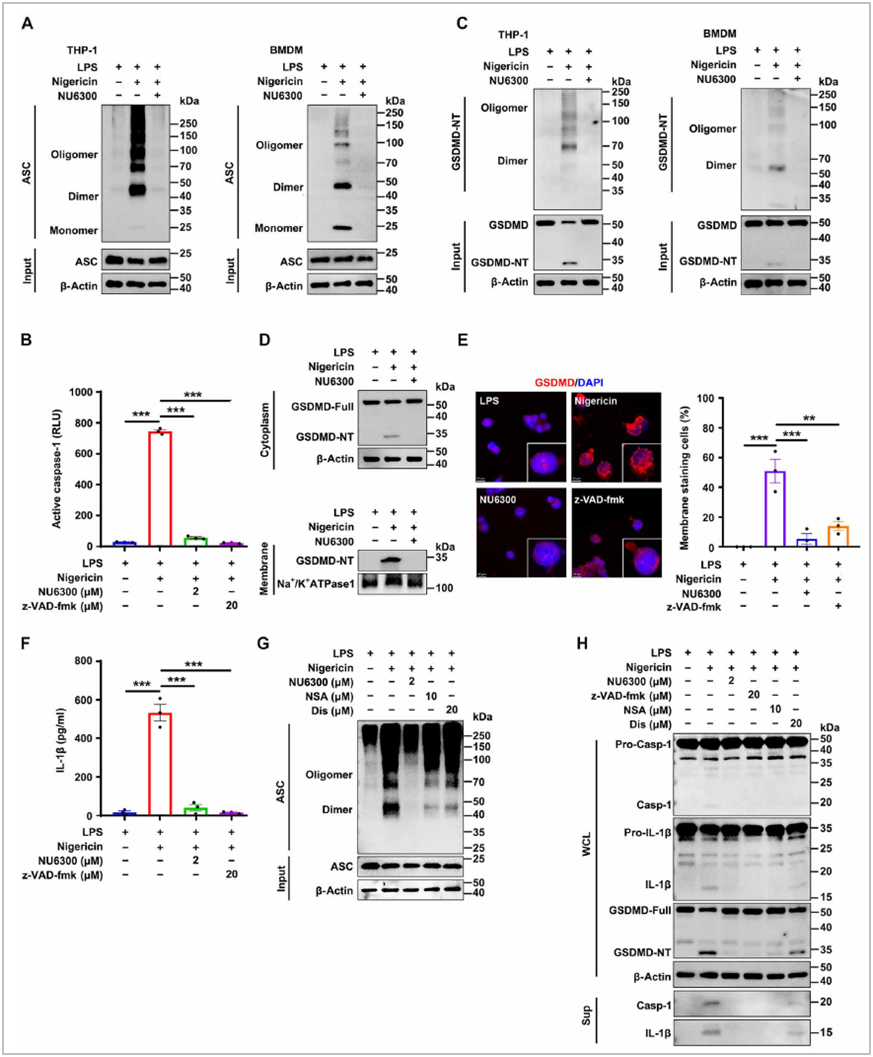
图6 GSDMD抑制剂对NLRP3炎症小体表现出反馈抑制作用
6、NU6300可减轻DSS诱导的小鼠结肠炎和LPS诱导的败血症
异常的炎症反应与多种病理状况有关,包括炎症性肠病和败血症。为了探索NU6300的治疗潜力,作者研究了对葡聚糖硫酸钠(DSS)诱导的结肠炎小鼠模型的影响,以及对LPS 诱导的脓毒症小鼠模型的影响,发现NU6300 大大改善了 DSS 诱导的结肠炎的严重程度,有效地免受LPS诱导的败血症的致命后果。为了检查 NU6300 的生存保护作用是否是由于GSDMD抑制所致,作者比较了野生型和GSDMD−/− C57BL/6J小鼠的生存情况,发现GSDMD-/−小鼠对LPS诱导的死亡有抵抗力,而 NU6300保护野生型小鼠免受LPS诱导的死亡,但没有显著影响GSDMD−/−小鼠的存活。结果表明GSDMD是NU6300对脓毒症模型保护作用的主要靶点(图7)。
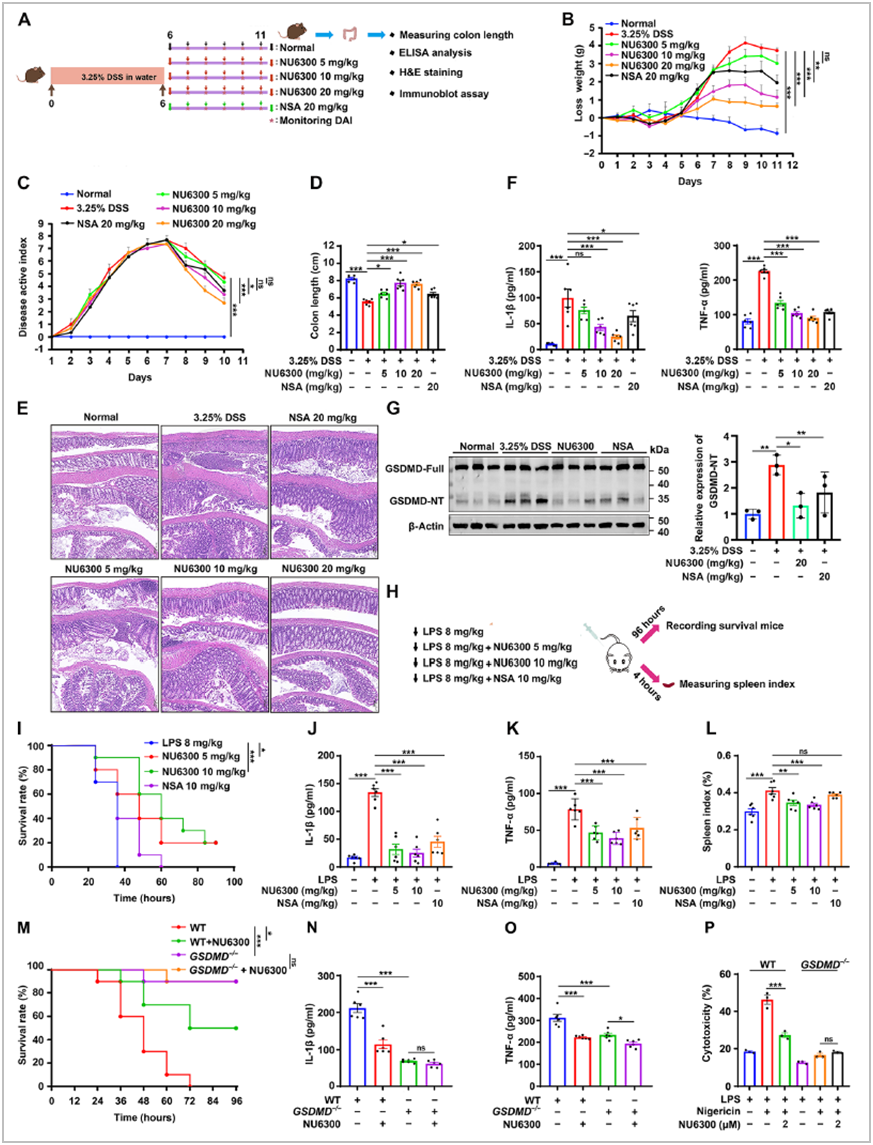
图7 NU6300减轻DSS诱导的小鼠结肠炎和LPS诱导的败血症
研究表明GSDMD 抑制剂NU6300在体外和体内均可减轻GSDMD介导的炎症。从机制上讲,NU6300与GSDMD的C191发生共价反应,阻断其裂解和棕榈酰化(图8)。GSDMD 的抑制作为炎症性焦亡疾病的治疗策略具有广阔的前景,而NU6300代表了一种有前途的治疗炎症性疾病的先导化合物。

















