Nature:肠道线粒体功能异常导致膳食脂质代谢紊乱
时间 : 2024-02-28线粒体功能障碍会诱发氧化磷酸化(OXPHOS)受阻和代谢缺陷,甚至导致严重疾病的发生。尽管线粒体疾病通常以脑肌病(encephalomyopathies)为人所知,但包括胃肠道(GI)在内的其他器官的稳态同样与线粒体功能密切相关。
肠上皮细胞是膳食脂肪吸收摄取的主要部位,摄取后的脂肪会在内质网中组装成前乳糜微粒,并被运输到高尔基体继续成熟形成乳糜微粒,最终分泌到循环系统中。目前,线粒体在肠上皮细胞膳食脂质处理中的作用尚不清楚,线粒体功能与胃肠道疾病间的关系也亟待研究。
近日,科隆大学Aleksandra Trifunovic和Manolis Pasparakis实验室合作在Nature杂志发表了题为 Mitochondrial dysfunction abrogates dietary lipid processing in enterocytes 的研究文章,发现线粒体功能障碍会导致膳食脂质从内质网到高尔基体的运输受阻,乳糜微粒的形成发生异常,从而导致膳食脂质大量储存于细胞质的脂滴中,脂质代谢紊乱。本研究揭示了肠上皮细胞的线粒体功能在膳食脂质处理中发挥了至关重要的作用。

为研究线粒体功能在肠道上皮细胞稳态维持中的作用及其对肠道生理的影响,作者在肠上皮细胞(IEC)中特异性敲除了对线粒体功能至关重要的天冬氨酰-tRNA合成酶编码基因DARS2(Dars2IEC-KO),发现敲除DARS2后肠上皮细胞增殖受阻,小鼠寿命变短,线粒体OXPHOS和电子传递异常,且肠上皮细胞中脂滴大量积累,脂肪含量上升。与Dars2IEC-KO小鼠类似,敲除SDHA(琥珀酸脱氢酶A,参与TCA循环和OXPHOS复合物II的酶)或Cox10(原卟啉IX法尼基转移酶,呼吸链复合物IV的组装因子)编码基因同样会导致肠上皮细胞中脂肪过度积累以及肠道上皮细胞增殖受阻。因此,线粒体功能障碍会导致肠上皮细胞中脂质运输发生障碍,脂肪过度积累。
为排除发育因素导致了Dars2IEC-KO小鼠的上述表型,作者利用Tamoxifen诱导型CreER重组酶诱导成年小鼠肠上皮细胞Dars2基因的特异性敲除,构建了Dars2tamIEC-KO小鼠模型。作者发现,Tamoxifen诱导5天会导致Dars2tamIEC-KO小鼠体重显著降低,诱导7天后发现OXPHOS和电子传递相关蛋白的表达下调。此外,尽管蛋白质组学分析发现Dars2tamIEC-KO小鼠的肠上皮细胞中脂质代谢途径下调,但与“脂滴形成”通路相关的蛋白表达上调。代谢组学分析发现Dars2tamIEC-KO小鼠近端小肠(负责吸收、加工和运输膳食脂肪)的上皮细胞中发生了严重的代谢紊乱:OXPHOS功能障碍,糖酵解活性异常增强,脂肪酸氧化受损。作者解剖Dars2tamIEC-KO小鼠肠道后发现近端小肠中脂肪大量积累,线粒体形态异常,随后的免疫组化发现增殖细胞、杯状细胞和吸收型肠细胞减少,干细胞标志物的表达也明显降低。因此,肠上皮细胞中诱导型DARS2敲除所导致的线粒体功能障碍致使肠上皮细胞发生了明显的代谢重编程,并引起了近端肠细胞中脂质的显著积累(图1)。
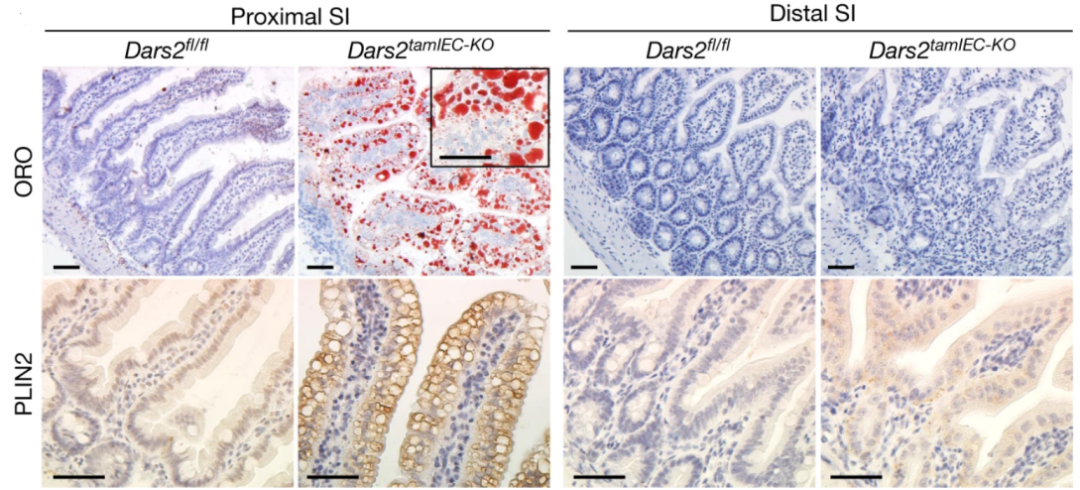
图1 Dars2突变会导致近端小肠脂滴异常积聚
基于Dars2tamIEC-KO小鼠的近端小肠的肠上皮细胞而非远端肠上皮细胞中积累了大量脂滴(图1),再加上脂质生物合成途径的整体下调,作者推测积累的脂质很可能主要来自膳食脂肪。为了评估膳食脂肪在此过程中的贡献,作者检测了无脂膳食喂养是否可以抑制Dars2tamIEC-KO小鼠肠上皮细胞中的脂质积累,发现与正常膳食相比,无脂膳食饲喂会显著减少DARS2缺陷型肠上皮细胞中LD的形成,从而证明了大多数积累的脂质来源于膳食。
接下来,作者利用代谢示踪实验评估了DARS2缺陷是否影响了肠上皮细胞对膳食脂质的运输。首先,作者发现Dars2tamIEC-KO小鼠的三油酸甘油酯、胆固醇和TAG的水平显著降低,表明DARS2缺陷抑制了肠上皮细胞对膳食脂质的运输,且肠细胞中丧失DARS2主要影响膳食脂质的处理。其次,Dars2tamIEC-KO小鼠的血浆甘油量上升,而腹腔和腹股沟白色脂肪组织的重量减少,表明脂肪组织的脂解反应上调,这可能是对膳食脂质供应受损的代偿性反应。第三,DARS2特异性敲除后,膳食脂质向循环系统的运输受阻。
大部分被肠上皮细胞吸收的膳食脂质会被包装到包含ApoB48的pre-CMs中,然后转运到高尔基体并分泌到胞外,以乳糜微粒(CM)的形式被运送到循环系统中。对照小鼠的CM广泛存在于肠上皮细胞的高尔基体囊泡内,或通过肠上皮的基底侧表面进行分泌。相比之下,Dars2tamIEC-KO小鼠的肠上皮细胞中CM分泌途径紊乱,高尔基体发生分散断裂,DARS2 缺陷会阻碍CM的产生并诱导进行性的高尔基体解构,从而导致 LD 在肠细胞中积累。为验证肠上皮细胞线粒体在膳食脂肪处理中的功能保守性,作者利用线虫模型探究了DARS2缺失对肠道高尔基体稳态的影响,同样发现肠上皮细胞中的线粒体功能缺陷会导致线虫脂质运输紊乱,而DARS2缺失会引起肠上皮细胞高尔基体分散断裂,抑制了脂质运输和嘌呤代谢,导致脂肪在肠细胞内的积聚。
综上所述,本研究发现肠上皮细胞中的线粒体功能障碍会诱发膳食脂质在内质网和高尔基体等部位的处理和运输异常,导致膳食脂质在胞浆脂滴中的积聚。本研究揭示了线粒体在肠上皮细胞膳食脂质代谢中的关键作用,对解析线粒体疾病患者的肠道病变发生机制具有重要意义。



